
 |
計算問題 |

 1/3
1/3


1 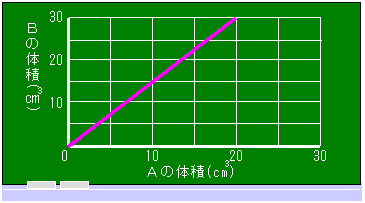 塩酸(A液)と水酸化ナトリウム水よう液(B液)をいろいろな割合で混ぜて、完全中和させました。そのときのA液・B液の体積は右のグラフのようになりました。これについて、次の問いに答えなさい。
塩酸(A液)と水酸化ナトリウム水よう液(B液)をいろいろな割合で混ぜて、完全中和させました。そのときのA液・B液の体積は右のグラフのようになりました。これについて、次の問いに答えなさい。
([問1]などのボタンをクリックすると、答えと解説があらわれます。)
A液18 を完全中和させるのに必要なB液は何 を完全中和させるのに必要なB液は何 ですか。 ですか。 |
| [問1]の答え | 27 | |
| 解説 |   1/2 1/2 |
|
 
グラフの、目もりとバッチリ重なっているところに注目しましょう。 Aが10  のとき、Bは15 のとき、Bは15 になっています。 になっています。A:B=10:15=2:3 です。 Aが20  のとき、Bは30 のとき、Bは30 になっています。 になっています。A:B=20:30=2:3 です。 AとBは、2:3で完全中和することがわかります。 |
||
A液50 にB液60 にB液60 を混ぜたものに、BTBを入れると何色になりますか。 を混ぜたものに、BTBを入れると何色になりますか。 |
| [問2]の答え | 黄色 | |
| 解説 |   1/4 1/4 |
|
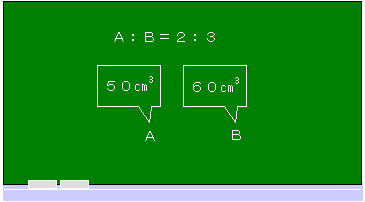 
グラフを読みとって、AとBの体積が、2:3のときに完全中和することがわかっています。 いま、Aは50  、Bは60 、Bは60 です。 です。
|
||

2 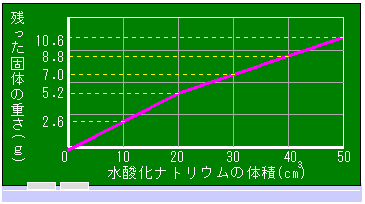 蒸発皿A〜Eに同じ塩酸50
蒸発皿A〜Eに同じ塩酸50 ずつをとり、同じ水酸化ナトリウム水よう液をAに10
ずつをとり、同じ水酸化ナトリウム水よう液をAに10 、Bに20
、Bに20 、Cに30
、Cに30 、Dに40
、Dに40 、Eに50
、Eに50 をそれぞれ加えました。その後、熱して水分を蒸発させて、残った固体の重さを調べると、右のグラフのようになりました。これについて、次の問いに答えなさい。
をそれぞれ加えました。その後、熱して水分を蒸発させて、残った固体の重さを調べると、右のグラフのようになりました。これについて、次の問いに答えなさい。
([問1]などのボタンをクリックすると、答えと解説があらわれます。)
| 蒸発皿A・蒸発皿Dにはそれぞれどんな物質が何gずつ残っていますか。 |
| [問1]の答え | A…食塩2.6g D…食塩5.2g、水酸化ナトリウム3.6g | |
| 解説 |   1/6 1/6 |
|
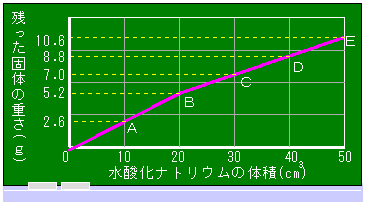 
まず、A〜Eの記号をグラフに書き込んでおきます。 そして、グラフの折れ曲がったところをさがします。 |
||
同じ塩酸100 ・水酸化ナトリウム水よう液80 ・水酸化ナトリウム水よう液80 を混ぜた後、熱して水分を蒸発させると何gの固体が残りますか。 を混ぜた後、熱して水分を蒸発させると何gの固体が残りますか。 |
| [問2]の答え | 17.6g | |
| 解説 |   1/16 1/16 |
|
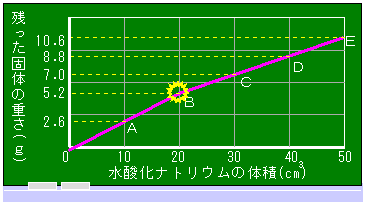 
この問題は、お手軽な解き方もありますが、いまは正々堂々と解いてみましょう。 そのためには、グラフをパーフェクトに読みとる必要があります。 読みとることは2つ。 1「完全中和したときの状態」 と、 2「水酸化ナトリウムのとけ方」 です。 |
||

3 水酸化ナトリウム20gを水にとかして、250 の水よう液にしました。この水よう液を20
の水よう液にしました。この水よう液を20 ずつとり6つの蒸発皿A〜Fにそれぞれ入れました。これらに、同じこさの塩酸の量をいろいろと変えて加えた後、それぞれの水分を蒸発させて、残った固体の重さを調べました。調べた結果は下の表のようになりました。これについて、次の問いに答えなさい。
ずつとり6つの蒸発皿A〜Fにそれぞれ入れました。これらに、同じこさの塩酸の量をいろいろと変えて加えた後、それぞれの水分を蒸発させて、残った固体の重さを調べました。調べた結果は下の表のようになりました。これについて、次の問いに答えなさい。

| 蒸発皿Aに残った固体の重さアは何gですか。 |
| [問1]の答え | 1.6g | |
| 解説 |   1/4 1/4 |
|
 
いろいろな解き方がありますが、もっとも簡単そうな解き方でやってみます。 |
||
水酸化ナトリウム水よう液20 を完全中和させるのに必要な塩酸は何 を完全中和させるのに必要な塩酸は何 ですか。 ですか。 |
| [問2]の答え | 37 | |
| 解説 |   1/7 1/7 |
|
 
まず、答えは「40  ではない」ことに注意してください。 ではない」ことに注意してください。A〜Dのところは、 「塩酸が5  増えると、 増えると、固体は0.1g増える」 となっているのでした。 |
||
| 蒸発皿Dに残った2.0gの固体の中には、水酸化ナトリウムは何gふくまれていますか。割り切れないときは、四捨五入して小数第2位まで求めなさい。 |
| [問3]の答え | 0.74g | |||||
| 解説 |   1/5 1/5 |
|||||
 
[問2]で、塩酸の体積が37  のときに、完全中和することがわかりました。 のときに、完全中和することがわかりました。ところが、いまは塩酸の体積が20  です。 です。
になっています。 |
||||||
