
 |
練習問題 |

 にした水よう液(A液とする)をつくった。
にした水よう液(A液とする)をつくった。 にした水よう液(B液とする)をつくった。
にした水よう液(B液とする)をつくった。 を水でうすめて、ちょうど100
を水でうすめて、ちょうど100 にした水よう(C液とする)をつくった。
にした水よう(C液とする)をつくった。 にB液を混ぜていくと、ちょうど60
にB液を混ぜていくと、ちょうど60 を入れたときに完全中和した。
を入れたときに完全中和した。 にC液を混ぜていくと、ちょうど80
にC液を混ぜていくと、ちょうど80 を入れたときに完全中和した。
を入れたときに完全中和した。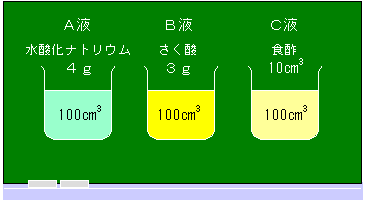
A液30 中にふくまれる水酸化ナトリウムは何gですか。また、B液60 中にふくまれる水酸化ナトリウムは何gですか。また、B液60 中にふくまれるさく酸は何gですか。 中にふくまれるさく酸は何gですか。 |
| [問1]の答え | 水酸化ナトリウム…1.2g、さく酸…1.8g | |
| 解説 |   1/2 1/2 |
|
 
A液100  中には、4gの水酸化ナトリウムがふくまれています。 中には、4gの水酸化ナトリウムがふくまれています。A液30  中には、 中には、30÷100=0.3(倍)の水酸化ナトリウムがふくまれているはずですから、 4×0.3=1.2(g)になります。 |
||
C液80 中にふくまれるさく酸は何gですか。 中にふくまれるさく酸は何gですか。 |
| [問2]の答え | 0.3g | |
| 解説 |   1/2 1/2 |
|
 
オより、 C液80  ←→ A液5 ←→ A液5 エの式を6で割ると、 A液5  ←→ B液10 ←→ B液10 よって、C液80  は、B液10 は、B液10 と同じはたらきをします。 と同じはたらきをします。
|
||
もとの食酢100 中には、何gのさく酸がふくまれていますか。 中には、何gのさく酸がふくまれていますか。 |
| [問3]の答え | 3.75g | |
| 解説 |   1/3 1/3 |
|
 
[問2]でわかったように、 C液80  中には、0.3gのさく酸がふくまれています。 中には、0.3gのさく酸がふくまれています。実際にはC液は100  ありますから、100÷80=1.25(倍)して、 ありますから、100÷80=1.25(倍)して、もとのC液には、 0.3×1.25=0.375(g)のさく酸がふくまれています。 |
||

2 塩酸と水酸化ナトリウム水よう液の中和を調べる実験をしました。これについて、次の問いに答えなさい。
( [問1]などのボタンをクリックすると、答えと解説があらわれます。)
<実験>
ア 水酸化ナトリウム60gを水にとかしてちょうど1Lの水よう液をつくった。
イ アの水よう液を100 ずつ蒸発皿に分けて、それぞれの蒸発皿に同じ塩酸を量を変えて加え、よく混ぜ合わせた。
ずつ蒸発皿に分けて、それぞれの蒸発皿に同じ塩酸を量を変えて加え、よく混ぜ合わせた。
ウ イのそれぞれの蒸発皿のよう液を熱して水分を蒸発させた。蒸発させた後、残った固体の重さと加えた塩酸の量の関係を調べると下のグラフのようになった。
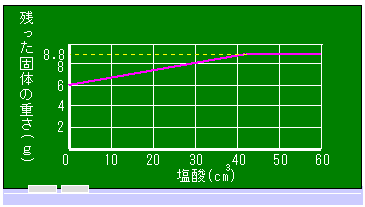
100 の水酸化ナトリウム水よう液を完全中和するのに必要な塩酸は何 の水酸化ナトリウム水よう液を完全中和するのに必要な塩酸は何 ですか。 ですか。 |
| [問1]の答え | 42 | |
| 解説 |   1/6 1/6 |
|
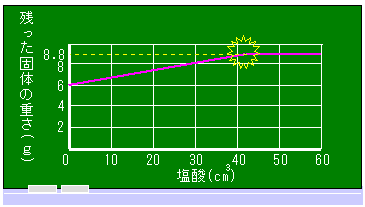 
完全中和するのは、グラフの折れ曲がったところです。 塩酸の体積は、40  よりもちょっと多いところですね。 よりもちょっと多いところですね。
|
||
100 の水酸化ナトリウム水よう液に塩酸27 の水酸化ナトリウム水よう液に塩酸27 を加えてよく混ぜた後、水を蒸発させて残る固体は何gですか。 を加えてよく混ぜた後、水を蒸発させて残る固体は何gですか。 |
| [問2]の答え | 7.8g | |
| 解説 |   1/3 1/3 |
|
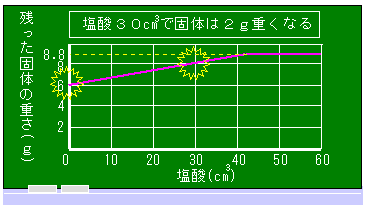 
[問1]で、塩酸が30  増えると、固体は2g重くなることがわかりました。 増えると、固体は2g重くなることがわかりました。
|
||
| [問2]で答えた固体の中で、食塩と水酸化ナトリウムはそれぞれ何gですか。割り切れないときは、四捨五入して小数第1位まで求めなさい。 |
| [問3]の答え | 食塩…5.7g、水酸化ナトリウム…2.1g | |
| 解説 |   1/5 1/5 |
|
 
この問題は、「残った固体のグラフ」から、「食塩の重さ」のグラフ、あるいは「水酸化ナトリウムのグラフ」を作って考えていきます。 どちらでも良いのですが、今は食塩の重さのグラフを書いて解いてみます。 |
||
